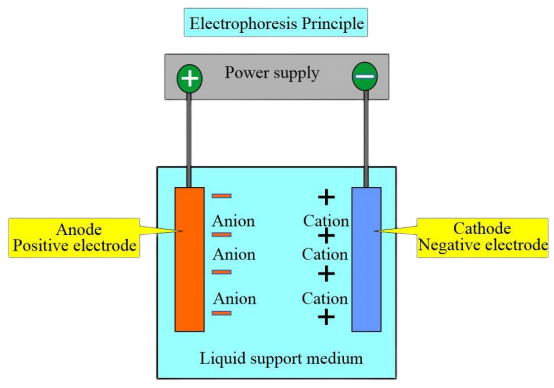
Princípio do Experimento
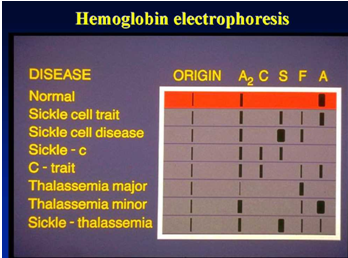
A eletroforese de hemoglobina visa detectar e confirmar várias hemoglobinas normais e anormais.
Devido às diferentes cargas e pontos isoelétricos dos diferentes tipos de hemoglobina, em uma determinada solução tampão de pH, quando o ponto isoelétrico da hemoglobina é inferior ao pH da solução tampão, a hemoglobina carrega uma carga negativa e migra em direção ao ânodo durante a eletroforese. Por outro lado, a hemoglobina com carga positiva move-se em direção ao cátodo.
Sob uma certa voltagem e após um tempo específico de eletroforese, hemoglobinas com diferentes cargas e pesos moleculares exibem diferentes direções e velocidades de migração. Isto permite a separação de zonas distintas, e subsequente análise de varredura colorimétrica ou eletroforética pode ser realizada nessas zonas para quantificar várias hemoglobinas. O método mais comumente usado é a eletroforese em membrana de acetato de celulose com pH 8,6.
Dentro do citoplasma, grupos etilenoglicol (CHOH-CHOH) presentes em glicogênio ou substâncias polissacarídicas (como mucopolissacarídeos, mucoproteínas, glicoproteínas, glicolipídeos, etc.) são oxidados pelo ácido periódico e convertidos em grupos aldeído (CHO-CHO). Esses grupos aldeídos combinam-se com o reagente de Schiff vermelho-púrpura incolor, formando um corante vermelho-púrpura que se deposita onde os polissacarídeos estão presentes na célula. Esta reação é conhecida como coloração com ácido periódico de Schiff (PAS), anteriormente conhecida como coloração com glicogênio.
Método Experimental
Materiais:Acetato de celulosemembrana, aparelho de eletroforese(DYCP-38C e fonte de alimentação DYY-6C), Ferramenta superior de carregamento de amostras (pipeta), espectrofotômetro, cubetas colorimétricas, buffers.
Tampão:
(1) Tampão TEB pH 8,6: Pesar 10,29 g de Tris, 0,6 g de EDTA, 3,2 g de ácido bórico e adicionar água destilada até 1000 ml.
(2) Tampão Borato: Pesar 6,87 g de bórax e 5,56 g de ácido bórico e adicionar água destilada até 1000 ml.
Procedimento:
Preparação da solução de hemoglobina
Tome 3 ml de sangue contendo heparina ou citrato de sódio como anticoagulante. Centrifugar a 2.000 rpm por 10 minutos e descartar o plasma. Lave os glóbulos vermelhos três vezes com solução salina fisiológica (750 rpm, 5 minutos de centrifugação de cada vez). Centrifugar a 2.200 rpm por 10 minutos e descartar o sobrenadante. Adicione uma quantidade igual de água destilada e, em seguida, adicione 0,5 vezes o volume de tetracloreto de carbono. Agite vigorosamente por 5 minutos e depois centrifugue a 2.200 rpm por 10 minutos para coletar a solução de Hb superior para uso posterior.
Imersão da Membrana
Corte a membrana de acetato de celulose em tiras medindo 3 cm x 8 cm. Mergulhe-os em tampão TEB pH 8,6 até ficarem totalmente saturados, depois remova e seque com papel de filtro.
Mancha
Use uma pipeta para colocar 10 μl da solução de hemoglobina verticalmente na membrana de acetato de celulose (o lado áspero), a cerca de 1,5 cm da borda.
Eletroforese
Despeje a solução tampão de borato na câmara de eletroforese. Coloque a membrana de acetato de celulose com o lado manchado na extremidade do cátodo da câmara. Execute a 200 V por 30 minutos.
Eluição
Recorte as zonas HbA e HbA2, coloque-as em tubos de ensaio separados e adicione 15 ml e 3 ml de água destilada, respectivamente. Agite suavemente para eluir completamente a hemoglobina e depois misture.
Colorimetria
Zere a absorvância utilizando água destilada para a solução de eluição e meça a absorvância a 415 nm.
Cálculo
HbA2(%) = Absorvância do tubo HbA2 / (Absorvância do tubo HbA × 5 + Absorvância do tubo HbA2) × 100%
Cálculo de Resultados Experimentais
Faixa de referência para eletroforese de acetato de celulose com tampão TEB de pH 8,6: HbA > 95%, HbA2 1%-3,1%
Notas
O tempo de eletroforese não deve ser muito longo. A membrana de acetato de celulose não deve secar durante a eletroforese. Pare a eletroforese quando a HbA e a HbA2 estiverem claramente separadas. A eletroforese prolongada pode causar difusão e desfoque da banda.
Evite usar muita amostra. O excesso de líquido de hemoglobina pode levar ao descolamento da banda ou à coloração insuficiente, resultando em níveis falsamente elevados de HbA1c.
Evitar a contaminação da membrana de acetato de celulose com proteínas.
A corrente não deve ser muito elevada; caso contrário, as bandas de hemoglobina poderão não se separar.
Sempre inclua amostras de indivíduos normais e hemoglobinas anormais conhecidas necessárias como controles.
A Beijing Liuyi Biotechnology fabrica o tanque de eletroforese profissional para eletroforese de hemoglobina que é o modeloDYCP-38Ctanque de eletroforese com membrana de acetato de celulose, e existem dois modelos de fonte de alimentação de eletroforese disponíveis para o tanque de eletroforese com membrana de acetato de celuloseDYY-2CeDYY-6Cfonte de energia.
Enquanto isso, a Beijing Liuyi Biotechnology fornece membrana de acetato de celulose para os clientes, e o tamanho da membrana de acetato de celulose pode ser personalizado. Bem-vindo ao nos pedir amostras e mais informações.
A marca Beijing Liuyi tem mais de 50 anos de história na China e a empresa pode fornecer produtos estáveis e de alta qualidade em todo o mundo. Através de anos de desenvolvimento, vale a pena sua escolha!
Agora estamos à procura de parceiros, tanto tanques de eletroforese OEM quanto distribuidores são bem-vindos.
Se você tiver algum plano de compra de nossos produtos, não hesite em nos contatar. Você pode nos enviar uma mensagem por e-mail[e-mail protegido]ou[e-mail protegido], ou ligue para +86 15810650221 ou adicione Whatsapp +86 15810650221, ou Wechat: 15810650221
Horário da postagem: 20 de setembro de 2023